リウマトイド因子とは?
関節リウマチにおけるリウマトイド因子の役割について詳しく知る
スクロールして見る
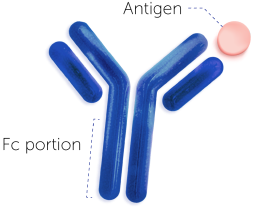
リウマトイド因子は、IgG抗体のFc領域と反応する自己抗体である1,2
関節リウマチにおけるリウマトイド因子は主にIgM、IgG、IgAのアイソタイプであるが、IgEおよびIgDも報告されている。1,3–5
関節リウマチ患者では、IgGに反応したB細胞が抗原に結合しやすいリウマトイド因子を産生する。6
これらのリウマトイド因子は、IgGのFc領域と結合することが可能である。1,6
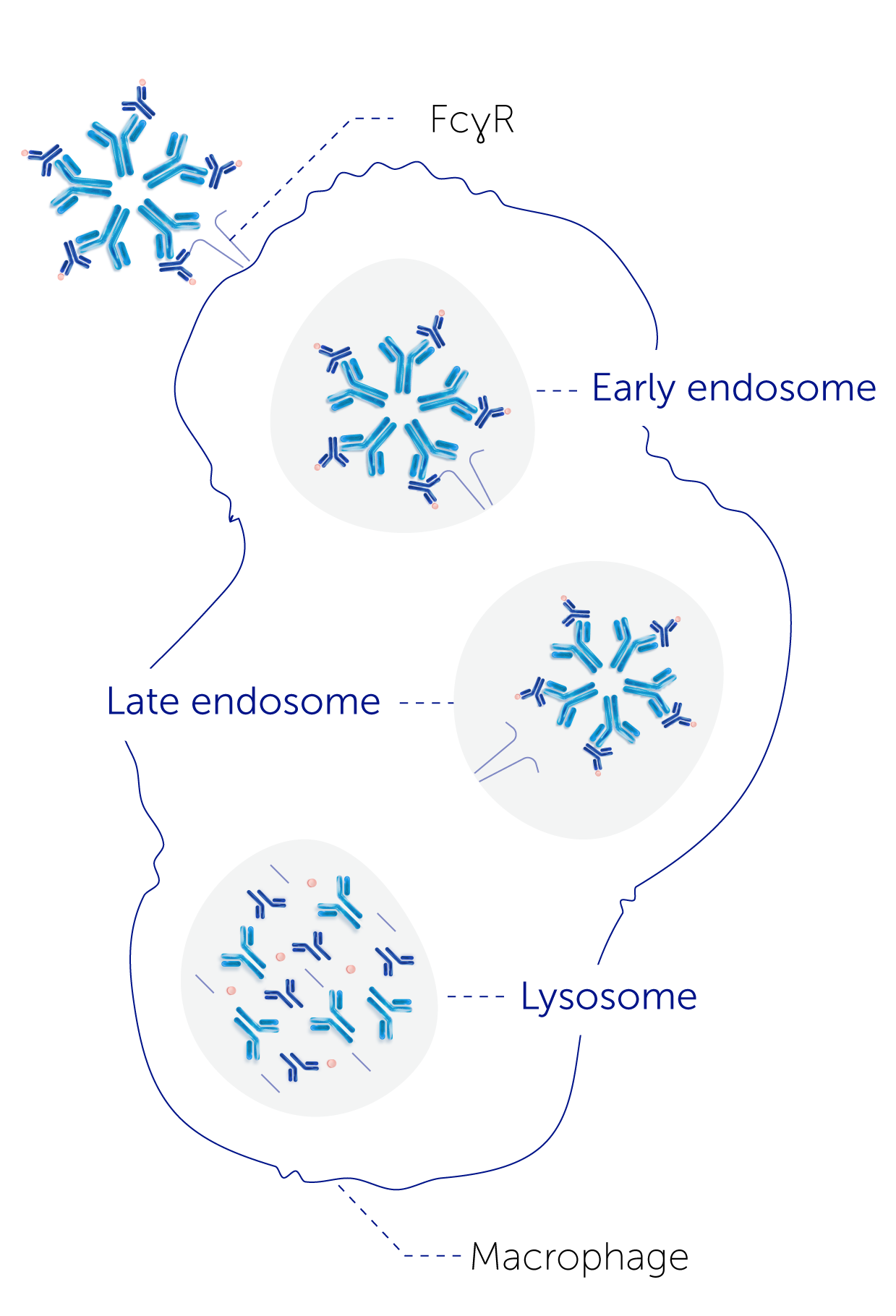
この結合により、大きな免疫複合体が形成される。4,6,7 免疫複合体は、Fcγ受容体を介してマクロファージに取り込まれ、リソソームによって分解される。4,8
title
Rheumatoid Factor
IgG Immunoglobulin
RF Immune Complex
Immune Complexes Are Degraded by Macrophages

関節リウマチ患者の70~90%は、リウマトイド因子に対して血清反応陽性である5,9–11
リウマトイド因子は医療機関で容易に検査可能であり、慢性炎症性関節疾患である関節リウマチの診断に有用である。3,5 関節リウマチは、その他のさまざまな症状や関節外症状を引き起こす。12,13
リウマトイド因子陽性は、リウマトイド因子高値とは異なる。リウマトイド因子高値を定義したガイドラインはなく、リウマトイド因子高値のカットオフ値は、臨床試験によって異なる。10,11,14–17
関節リウマチ患者の約4人に1人は、200IU/ml超のリウマトイド因子高値である。15–17
関節リウマチにおけるリウマトイド因子について理解を深める
リウマトイド因子の値が特に高い場合、関節リウマチの予後不良因子と考えられる18-20
リウマトイド因子が高い関節リウマチ患者は、以下の可能性が高くなる:
- 症状の悪化18-21
- 進行しやすく放射線学的進行リスクが高い21–23
- 高い疾患活動性21
- 低寛解率21
- 関節外症状の高い有病率22,24は 関節破壊や身体障害の予後不良と関連25
- 心血管疾患関連死亡率の リスク増加26
- Abbreviations: EU: European Union; Fc: fragment crystallizable; FcγR: Fc-gamma receptor; Ig: immunoglobulin; RF: rheumatoid factor; SpA: spondyloarthritis; US: United States.
- References: 1. Maibom-Thomsen SL, et al. PLoS One. 2019;14(6):e0217624; 2. Kanmert D, et al. Scand J Immunol. 2012;75(1):115–9; 3. van Delft MAM, Huizinga TWJ. J Autoimmun. 2020;110:102392; 4. Levy RA, et al. Immunotherapy. 2016;8(12):1427–36; 5. Ingegnoli F, et al. Dis Markers. 2013;35(6):727–34; 6. Nicolò A, et al. Front Immunol. 2022;13:1016263; 7. Lamers MC. Allergy. 1981;36(8):527–35; 8. Junker F, et al. Front Immunol. 2020;11:1393; 9. Wu CY, et al. Int J Mol Sci. 2021;22(2):686; 10. Nielsen SF, et al. BMJ. 2012;345:e5244; 11. Smolen JS, et al. Ann Rheum Dis. 2009;68(6):797–804; 12. Sparks JA. Ann Intern Med. 2019;170(1):ITC1–ITC16; 13. Smolen JS, et al. Lancet. 2016;388(10055):2023–38; 14. Kratz A, et al. N Engl J Med. 2004;351(15):1548–63; 15. Atsumi T, et al. Ann Rheum Dis. 2016;75(1):75–83; 16. Smolen JS, et al. Lancet. 2016;388(10061):2763–74; 17. Tanaka Y, et al. Int J Rheum Dis. 2023;26(7):1248–59; 18. Albrecht K, Zink A. Arthritis Res Ther. 2017;19(1):68; 19. Smolen JS, et al. Ann Rheum Dis. 2023;82(1):3–18; 20. Aletaha D, et al. Arthritis Rheum. 2010;62(9):2569–81; 21. Sobhy N, et al. Egypt Rheumatol. 2022;44(4):325–8; 22. van Zeben D, et al. Ann Rheum Dis. 1992;51(9):1029–35; 23. Vastesaeger N, et al. Rheumatology (Oxford). 2009;48(9):1114–21; 24. Cojocaru M, et al. Maedica (Bucur). 2010;5(4):286–91; 25. Nell VPK, et al. Ann Rheum Dis. 2005;64(12):1731–6; 26. England BR, et al. Arthritis Care Res (Hoboken). 2016;68(1):36–45.